RIVAROXABAN
Pagina pubblicata il 11/04/2012 – ultimo aggiornamento: 12/10/2023
NOME COMMERCIALE E FORMULAZIONI
-
XARELTO cpr 2,5 mg
- XARELTO cpr 10 mg
- XARELTO cpr 15 mg
- XARELTO cpr 20 mg
Rivaroxaban su PubChem, il database open della chimica
Nome IUPAC: 5-chloro-N-[[(5S)-2-oxo-3-[4-(3-oxomorpholin-4-yl)phenyl]-1,3-oxazolidin-5-yl]methyl]thiophene-2-carboxamide
Formula chimica: C19H18ClN3O5S
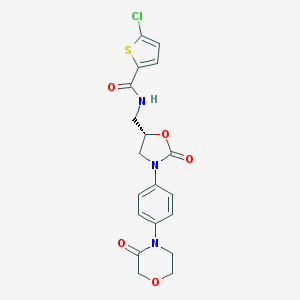
Rivaroxaban – formula di struttura (fonte: PubChem)
SCHEDA TECNICA XARELTO (RCP) fonte: EMA -12/10/2023
riassunto della relazione pubblica europea di valutazione per Xarelto destinata al pubblico
INDICAZIONI (Xarelto 2,5 mg):
Xarelto, somministrato insieme con il solo acido acetilsalicilico (acetylsalicylic acid, ASA) o con ASA e clopidogrel o ticlopidina, è indicato per la prevenzione di eventi aterotrombotici in pazienti adulti dopo una sindrome coronarica acuta (SCA) con biomarcatori cardiaci elevati (vedere paragrafi 4.3, 4.4 e 5.1 dell’RCP).
Xarelto, somministrato insieme con acido acetilsalicilico (ASA), è indicato per la prevenzione di eventi aterotrombotici in pazienti adulti, ad alto rischio di eventi ischemici, che presentano coronaropatia (coronary artery disease, CAD) o arteriopatia periferica (peripheral artery disease, PAD) sintomatica.
INDICAZIONI (Xarelto 10 mg):
Prevenzione del tromboembolismo venoso (TEV) nei pazienti adulti sottoposti a interventi di sostituzione elettiva di anca o di ginocchio.
Trattamento della trombosi venosa profonda (TVP) e dell’embolia polmonare (EP) e prevenzione delle recidive di TVP ed EP nell’adulto. (Vedere paragrafo 4.4 dell’RCP per pazienti EP emodinamicamente instabili.)
INDICAZIONI (Xarelto 15 mg e 20 mg):
Adulti
Prevenzione dell’ictus e dell’embolia sistemica nei pazienti adulti affetti da fibrillazione atriale non valvolare con uno o più fattori di rischio, come insufficienza cardiaca congestizia, ipertensione, età ≥ 75 anni, diabete mellito, pregresso ictus o attacco ischemico transitorio.
Trattamento della trombosi venosa profonda (TVP) e dell’embolia polmonare (EP) e prevenzione delle recidive di TVP ed EP nell’adulto. (vedere paragrafo 4.4 per pazienti EP emodinamicamente instabili)
Popolazione pediatrica
Trattamento del tromboembolismo venoso (TEV) e prevenzione delle recidive di TEV nei bambini e negli adolescenti di età inferiore a 18 anni e peso compreso tra 30 kg e 50 kg dopo almeno 5 giorni di trattamento anticoagulante parenterale iniziale.
CONTROINDICAZIONI (Xarelto 2,5 mg, 10 mg, 15 mg e 20 mg)
Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1 dell’RCP.
Emorragie clinicamente significative in atto.
Lesioni o condizioni tali da costituire un rischio significativo di sanguinamento maggiore. Queste possono includere ulcerazione gastrica recente o in corso, presenza di neoplasie maligne ad alto rischio di sanguinamento, recente traumatismo cerebrale o spinale, intervento chirurgico cerebrale, spinale od oftalmico, recente emorragia intracranica, varici esofagee accertate o sospette, malformazioni arteriovenose, aneurismi vascolari o disfunzioni vascolari maggiori a livello intraspinale o intracerebrale.
Trattamento concomitante con altri anticoagulanti, come le eparine non frazionate, le eparine a basso peso molecolare (enoxaparina, dalteparina, ecc.), i derivati dell’eparina (fondaparinux, ecc.), gli anticoagulanti orali (warfarin, dabigatran etexilato, apixaban, ecc.), tranne nel caso di cambiamento di terapia anticoagulante (vedere paragrafo 4.2) o quando le eparine non frazionate siano somministrate a dosi necessarie per mantenere in efficienza un catetere centrale aperto, venoso od arterioso (vedere paragrafo 4.5 dell’RCP).
Patologie epatiche associate a coagulopatia e rischio emorragico clinicamente significativo, compresi i pazienti cirrotici con Child Pugh B e C.
Gravidanza e allattamento (vedere paragrafo 4.6 dell’RCP).
Solo 2,5 mg:
Trattamento concomitante della SCA con terapia antipiastrinica in pazienti con pregresso ictus o attacco ischemico transitorio (transient ischaemic attack, TIA) (vedere paragrafo 4.4 dell’RCP).
Trattamento concomitante di CAD/PAD con ASA in pazienti con pregresso ictus emorragico o lacunare, o ictus di qualsiasi tipo nel mese precedente (vedere paragrafo 4.4 dell’RCP).
Meccanismo d’azione
Rivaroxaban è un inibitore diretto e altamente selettivo del fattore Xa, con biodisponibilità orale. L’inibizione del fattore Xa interrompe le vie intrinseca ed estrinseca della cascata della coagulazione e inibisce sia la formazione di trombina, sia lo sviluppo di trombi. Rivaroxaban non inibisce la trombina (fattore II attivato) e non ne è stato dimostrato alcun effetto sulle piastrine. (fonte: RCP)
Nota Informativa Importante AIFA sui nuovi anticoagulanti orali Eliquis, Pradaxa, Xarelto e Lixiana(20/05/2019)
“Apixaban (Eliquis), dabigatran etexilato (Pradaxa), edoxaban (Lixiana/Roteas) e rivaroxaban (Xarelto) non sono raccomandati nei pazienti con sindrome antifosfolipidica a causa del possibile aumento del rischio di eventi trombotici ricorrenti.”
La nota infornativa importante AIFA sui NAO e rischio di eventi trombotici in pz con APS da QUI
DETERMINA AIFA 1 marzo 2019
COSTO E RIMBORSABILITA’
- XARELTO 10 mg compresse rivestite con film – uso orale – blister (PP/ALU) 5 compresse
- Classe di rimborsabilita’: A.
- Prezzo ex factory (IVA esclusa): € 11,60.
- Prezzo al pubblico (IVA inclusa): € 19,14
- XARELTO 10 mg compresse rivestite con film – uso orale – blister (PP/ALU) 10 compresse
- Classe di rimborsabilita’: A.
- Prezzo ex factory (IVA esclusa): € 23,20.
- Prezzo al pubblico (IVA inclusa): € 38,29.
- XARELTO 10 mg compresse rivestite con film – uso orale – blister (PP/ALU) 30 compresse
- Classe di rimborsabilita’: A.
- Prezzo ex factory (IVA esclusa): € 69,60.
- Prezzo al pubblico (IVA inclusa): € 114,87.
DETERMINA AIFA 1 ottobre 2014
COSTO E RIMBORSABILITA’
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister – 14 compresse.
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 32,48.
- Prezzo al pubblico (IVA inclusa): € 53,60;
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 28 compresse.
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 64,96.
- Prezzo al pubblico (IVA inclusa): € 107,21;
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 42 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 97,44.
- Prezzo al pubblico (IVA inclusa): € 160,81;
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 98 compresse
- Classe di rimborsabilità: «C»;
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 10×1 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 23,20.
- Prezzo al pubblico (IVA inclusa): € 38,29;
- XARELTO 15 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 100×1 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 232,20.
- Prezzo al pubblico (IVA inclusa): € 382,90;
- XARELTO 20 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 14 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 32,48.
- Prezzo al pubblico (IVA inclusa): € 53,60;
- XARELTO 20 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 28 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 64,96.
- Prezzo al pubblico (IVA inclusa): € 107,21;
- XARELTO 20 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 98 compresse
- Classe di rimborsabilità: «C»;
- XARELTO 20 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 10×1 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 23,20.
- Prezzo al pubblico (IVA inclusa): € 38,29;
- XARELTO 20 mg – compressa rivestita con film – uso orale – blister (PP/ALU) – 100×1 compresse
- Classe di rimborsabilità: «A».
- Prezzo ex factory (IVA esclusa): € 232,00.
- Prezzo al pubblico (IVA inclusa): € 382,90.
Nota informativa importante AIFA sui nuovi anticoagulanti orali Eliquis, Pradaxa, Xarelto (11/09/2013)
” L’Agenzia Italiana del Farmaco rende disponibile nuove e importanti informazioni sui fattori di rischio per il sanguinamento – Prestare attenzione alla posologia, alle controindicazioni e alle avvertenze speciali e precauzioni d’impiego per ridurrne il rischio.
Eliquis (apixaban), Pradaxa (dabigatran etexilato) e Xarelto (rivaroxaban) sono anticoagulanti orali che hanno recentemente ricevuto l’autorizzazione per indicazioni per le quali vengono usati da decenni gli antagonisti della vitamina K (warfarin, fenprocumone e acenocumarolo) o le eparine a basso peso molecolare (EBPM). A differenza degli antagonisti della vitamina K, questi nuovi medicinali non richiedono il monitoraggio di routine dell’attività anticoagulante.
Tuttavia, negli studi clinici e nell’esperienza post-marketing è stato dimostrato che gli eventi di sanguinamento maggiore, inclusi eventi fatali, non sono limitati al solo uso degli antagonisti della vitamina K/EBPM ma sono rischi significativi anche per i nuovi anticoagulanti orali.”
La Nota informativa AIFA in PDF da QUI
Rivaroxaban su PubMed ==> da QUI
Segnalo come piuttosto interessante il lavoro: “The EINSTEIN-PE Investigators Oral Rivaroxaban for the Treatment of Symptomatic Pulmonary Embolism. N Engl J Med 2012, Mar 26 “; Il gruppo di ricerca del programma EINSTEIN-PE ha concluso uno studio multicentrico randomizzato di “non inferiorità” in un grosso gruppo di soggetti con embolia polmonare acuta sintomatica, con o senza trombosi venosa profonda. Sono stati valutati l’efficacia e la percentuale di eventi avversi di un trattamento con l’inibitore orale del Fattore Xa rivaroxaban (15 mg due volte al giorno per 3 settimane, seguiti da 20 mg una volta al giorno) vs terapia standard con enoxaparina seguita da un antagonista della vitamina K per 3, 6 o 12 mesi. I risultati hanno dimostrato una “non inferiorità” del rivaroxaban rispetto alla terapia tradizionale e una sovrapponibilità della percentuale degli eventi avversi, tranne per i sanguinamenti maggiori che si sono manifestati con una frequenza inferiore. >>>>>>>>>>>>>>>>>> da QUI il link per l’abstract
Rivaroxaban sul sito della FDA
Rivaroxaban sul sito della Cochrane
Rivaroxaban su Google Scholar (Ricerca globale)
Rivaroxaban su Google Scholar (Ricerca in lingua italiana)
medicinale soggetto a prescrizione medica (RR).
Condizioni e modalità di impiego
Per l’indicazione terapeutica:
Con determina AIFA del 17/06/2020, per un periodo di 120 giorni, salvo ulteriori proroghe, il farmaco XARELTO è stato reso prescrivibile da specialisti e Medici di Medicina Generale, secondo le indicazioni della NOTA AIFA n. 97 per il trattamento della fibrillazione atriale non valvolare (FANV)
Prevenzione del tromboembolismo venoso (TEV) nei pazienti adulti sottoposti a interventi di sostituzione elettiva di anca o di ginocchio. Prescrizione del medicinale di cui all’allegato 2 e successive modifiche, alla determinazione 29 ottobre 2004 – PHT Prontuario della distribuzione diretta -, pubblicata nel supplemento ordinario alla Gazzetta Ufficiale n. 259 del 4 novembre 2004.
Per le indicazioni terapeutiche:
Prevenzione dell’ictus e dell’embolia sistemica nei pazienti adulti affetti da fibrillazione atriale non valvolare con uno o piu’ fattori di rischio, come insufficienza cardiaca congestizia, ipertensione, eta’ >=75 anni, diabete mellito, pregresso ictus o attacco ischemico transitorio. Trattamento della trombosi venosa profonda (TVP) e dell’embolia polmonare (EP) e prevenzione delle recidive di TVP ed EP nell’adulto (vedere paragrafo 4.4 per pazienti EP emodinamicamente instabili).
Prescrizione del medicinale soggetta a diagnosi – piano terapeutico e a quanto previsto dall’allegato 2 e successive modifiche, alla determinazione 29 ottobre 2004 – PHT Prontuario della distribuzione diretta -, pubblicata nel supplemento ordinario alla Gazzetta Ufficiale n. 259 del 4 novembre 2004.
Farmaco sottoposto a monitoraggio intensivo delle reazioni avverse
Dott. Salvatore Nicolosi
Medico di Medicina Genarale convenzionato con il S.S.N.